会“造血”的贝壳—颠覆演化史的“活盔甲”

在动物界中,骨骼大致可以分为两类。一类是我们人类所属的脊椎动物拥有的“内骨骼”,这具骨骼不仅是身体的支架,其内部的骨髓更是一座不知疲倦的“生命工厂”,持续不断地生产着血液和免疫细胞,是名副其实的“造血活器官”。另一类则是更为庞大的无脊椎动物群体,如贝类、虾蟹等披挂在外各式各样的“外骨骼”。长期以来,生物学的经典观点认为,这些外骨骼如同古代将士的盔甲,是贝类等分泌形成的坚硬矿物保护层,一旦成型便不再参与核心的生命活动。
然而,正是这个看似清晰的划分,在面对生命演化史上最大的谜题之一——“寒武纪动物大爆发”时,显得有些力不从心。在大约5.4亿年前,地球上拥有矿化骨骼的动物在短时间内爆炸式地涌现,迅速奠定了当今动物界多样性的基础蓝图。一个关键问题始终困扰着科学家们:如果这些最早出现的、占据了绝对数量优势的外骨骼仅仅是一副“无生命的盔甲”,它们是如何为远古动物提供足够强大的演化优势,从而驱动这场波澜壮阔的生命奇迹的?
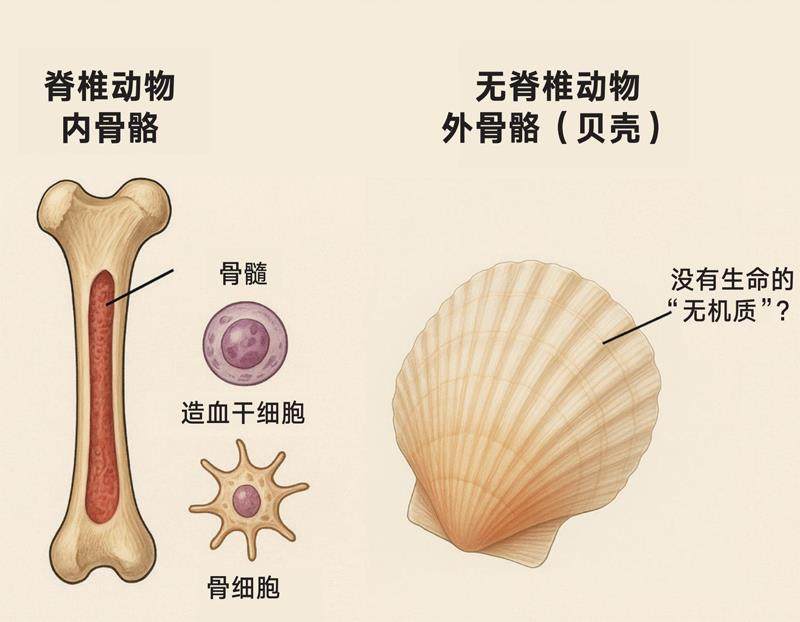
近年来,这一困扰学界百年的“悬案”终于获得了新线索。来自中国海洋大学专门攻坚贝类的研究团队,通过一系列严谨的科学实验取得的成果,在国际上首次揭示了一个颠覆性的事实:在无脊椎动物的骨骼中,普遍存在着功能活跃的造血干细胞巢。这项发表于国际权威期刊的最新成果,直接挑战了“骨骼造血为脊椎动物所特有”的传统观念。它不仅明确了贝壳等外骨骼也是“造血活器官”,更为我们重新理解动物造血系统的起源、骨骼的演化,乃至寒武纪动物大爆发的原因,提供了强有力的全新证据。
叩响未知之门:贝壳中的生命信号
科学探索创新的道路,往往由一些看似无关的“意外”铺就。软体动物,是海洋中最大的动物门类,也是寒武纪早期起源的主要矿化骨骼动物类群之一。在正式揭开贝壳的“生命之谜”前,中国和国际上的一些学者早已注意到,这些被人们定义为“无生命”的贝壳,在实验中却能展现出诸多令人费解的生物学特性。例如,曾有研究报道指出,将贝壳粉末作为细胞培养的添加物,能显著提高脊椎动物干细胞的活性,甚至促进成骨细胞的矿化。这些现象说明,贝壳与脊椎动物具有造血功能的“活骨骼”之间,也许存在着更加紧密的、超越外在区别的关联。但这些零散的线索,始终难以用传统理论给出一个令人信服的解释。
破解谜题的关键突破口,源于实验中的偶然。在一次实验操作中,研究团队按照常规软体组织核酸提取方法,处理新鲜扇贝组织的同时,也处理了贝壳。按常理来说,贝壳的主要成分为碳酸钙,不应含有大量的生物大分子。然而,在后续的检测中,一个意想不到的结果出现了:仪器清晰地显示,从这些被仔细清理过的贝壳样本中,竟然检测到了大量具有生物活性的RNA(核糖核酸)分子。
RNA是执行生命功能的核心信息分子,它富有活性是细胞仍在进行生命活动的最直接证据。这一意想不到的实验结果,为研究团队提供了一个崭新的线索。它意味着,贝壳内部并非传统观念中那样全为矿物质,而是蕴藏着数量庞大的活细胞。这个发现虽然令人振奋,但随之而来的是一个巨大的技术挑战:如何在不破坏细胞的前提下,深入到坚硬、不透明的贝壳内部,去探寻这些神秘细胞的真实身份和功能?这在当时难住了科学家们。面对这一前所未有的研究“禁区”,团队下定决心,必须啃下这块“硬骨头”,去揭开贝壳内部隐藏的生命奥秘。
解密“活盔甲”:贝壳内的“类骨髓”干细胞巢
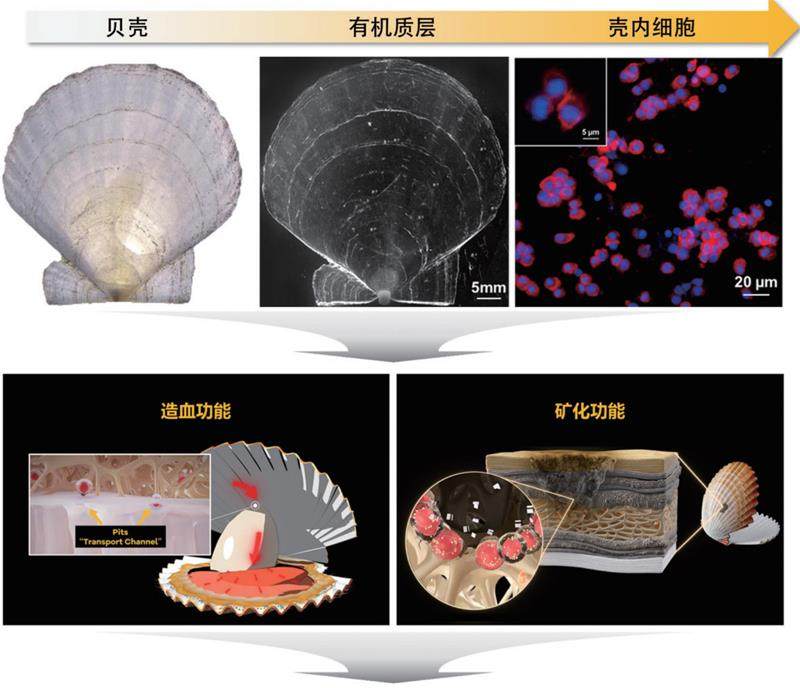
为了“看清”贝壳里的细胞,研究团队踏上了一条漫长而艰辛的技术攻关之路。他们深知,需要建立一套全新的实验体系,才能既去除贝壳坚硬的矿物质,又最大限度地保留内部细胞的活性和原始结构。经过数年艰辛的摸索与尝试,团队最终成功建立了一套国际领先的、适用于无脊椎动物外骨骼的干细胞研究体系。凭借这一核心技术,他们终于能够将完整的贝壳内部组织结构清晰地呈现在显微镜下。
通过多组学遗传学分析、细胞体外培养、活体动物细胞示踪等一系列系统性的功能验证,一个颠覆性的事实被明确地证实了:在扇贝等贝类的外骨骼(贝壳)内部,广泛存在着一个由多种细胞构成的、功能高度活跃的造血干细胞巢。这个发现于今年正式发表在国际权威学术期刊《科学进展》上,立即引起了国际学术界的广泛关注。
这个位于贝壳内的造血干细胞巢,可以说是无脊椎动物的“骨髓”。它不仅是其体内循环的免疫细胞(血细胞)的发源地,其诸多生物学特性也与脊椎动物的骨髓造血微环境高度相似。这意味着,贝壳不仅仅是一副外在的“盔甲”,其内部更是一座能够主动制造“国防力量”的“活体兵工厂”。这一原创性发现,在国际上首次揭示了无脊椎动物骨骼中存在普适性的干细胞巢,彻底颠覆了“骨骼造血功能为脊椎动物特有演化”的传统观念。更进一步的研究揭示,这些“贝壳骨髓”至少在四个方面表现出独特的研究价值。
高丰度的造血干细胞及其对再生医学的启示
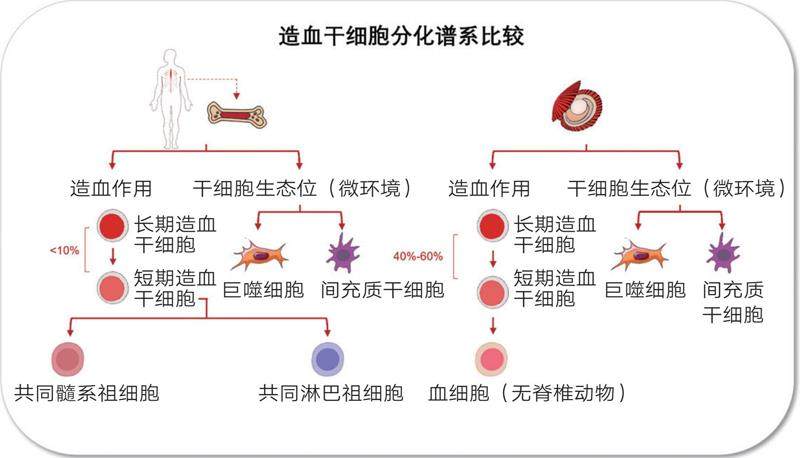
研究发现,贝壳内造血干细胞的丰度高得惊人,其比例可达40%至60%。与之形成鲜明对比的是,在高等脊椎动物的骨髓中,造血干细胞或前体细胞的比例通常极低(小于<10%)。贝壳如同一个天然、高效的“干细胞孵化器”。深入理解其独特的高比例干细胞维持机制,有望为再生医学领域,特别是为突破体外干细胞的扩增与培养技术瓶颈,提供重要的理论启示和全新的研究思路。
造血谱系的古老同源性
研究团队通过基因组学特征分析、遗传调控机制追溯、干细胞微环境对比以及发育分化功能验证等多个维度的系统性研究,均证实了贝壳的造血系统与高等脊椎动物的造血结构功能具有高度的相似性。这一系列证据共同指向了一个结论:骨骼造血系统并非脊椎动物在演化中后期才出现的“高等”创新,它的起源远比我们想象的要古老,可能在数亿年前的共同祖先身上就已具有雏形。这为理解整个动物界造血系统的起源与演化提供了至关重要的参考。
“造血-矿化”的双潜能分化机制
研究中一个极为有趣的发现是,这些贝壳内的造血干细胞竟然是“身兼数职”的多面手。它们不仅能分化为血液细胞,执行“造血”功能;还能分化为成壳细胞,执行“生物矿化”功能,负责贝壳的生长、修复与再生。这一发现,不仅挑战了人们传统上认为贝壳矿化仅由外套膜组织负责的观点,更在细胞和功能层面上,首次揭示了动物“造血”与“矿化”这两大核心生命过程之间,存在着深刻的、源自祖先的内在演化联系。
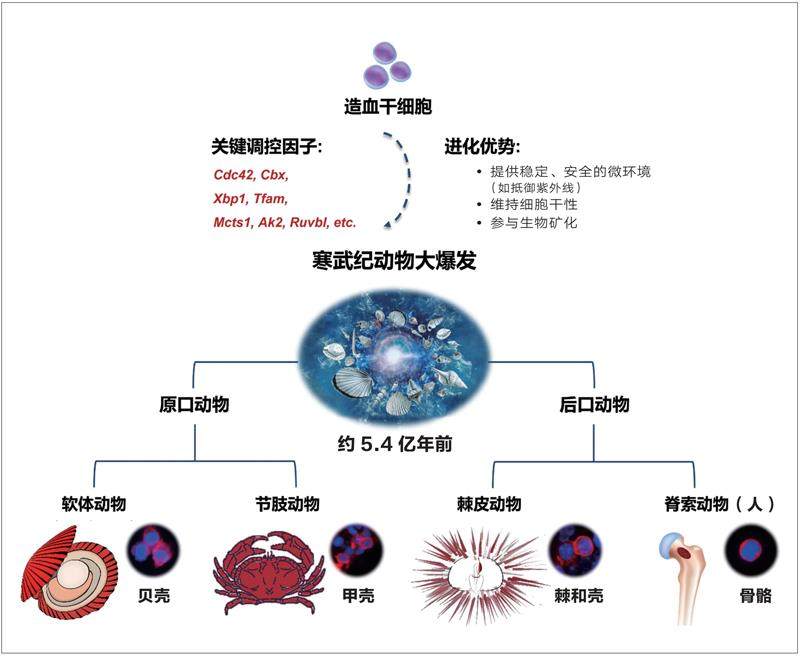
骨骼造血的跨物种保守性
为了验证这一发现的普遍性,团队的研究并未止步于扇贝。他们将研究拓展至牡蛎、鲍鱼等其他贝类,乃至海胆等棘皮动物。结果显示,在这些拥有矿化骨骼的无脊椎动物类群中,均能发现功能相似的造血干细胞巢。这一跨物种的保守性规律表明,“骨骼干细胞巢”的出现,可能是寒武纪动物大爆发时期,各类群动物能够快速演化出多样化形态和生存策略的重要内在驱动力之一。穿上了这身“活盔甲”,远古动物才获得了前所未有的生存与演化优势。
开启应用新蓝海
从在贝壳中发现“准骨髓”,到追溯贝壳中的干细胞参与了“造血”与“矿化”的双重功能,中国海洋大学研究团队这项里程碑式的发现,环环相扣,为我们揭示了动物骨骼细胞从起源到生理功能构建的完整演化图景,系统性地重构了我们对动物造血系统和骨骼演化历史的认知。
这一基础科学领域的重大突破,其深远影响已远远超出了演化生物学本身,正向更广阔UyAksq1NPG3bZzGTdiVZBZW0bF6Umf6b0JVV2qqDhNM=的应用领域辐射,展现出多方面的应用潜力。在基础医学领域,贝壳独特的干细胞巢为研究白血病、再生障碍性贫血、骨质疏松等与造血、骨骼相关的疾病UyAksq1NPG3bZzGTdiVZBZW0bF6Umf6b0JVV2qqDhNM=,提供了一种全新的、极具价值的研究模型,有望催生新的治疗思路和药物靶点。
而在蓝色经济领域,这些发现更是直接的“生产力”。掌握了调控贝类免疫(造血)和生长(矿化)的核心基因资源,就意味着我国的水产科技工作者能够运用现代生物技术,进行更精准、更高效的遗传改良。未来,人们可以实现干细胞设计育种,培育出生长更快、品质更好、抗病力更强、经济性状更优良的扇贝、牡蛎等水产贝类新品种。这将不再是遥不可及的梦想,并且对于保障我国水产品的稳定供给、推动海水养殖产业的绿色可持续发展,具有不可估量的战略意义。
一枚贝壳上,浓缩了数亿年演化智慧的“年轮”。它沉默地见证了地球生命演进的壮阔历程,如今,又在中国科学家的手中,向我们揭示了关乎寒武纪动物大爆发的深刻奥秘。这正是基础科学研究的魅力所在:它源于对自然的好奇,勇于挑战权威与定论,并最终在探索未知的过程中,为人类社会的未来发展,提供源源不断的创新动力。
(作者单位:中国海洋大学)
[责任编辑]龚婷